HLB 주가는 27일 전일 대비 9.34% 상승한 9만2500원에 장을 마쳤다. 이날 주가 강세 배경에는 간암 신약 ‘리보캄렐 병용요법’이 세계적인 암학회인 유럽종양학회(ESMO)의 공식 치료 가이드라인에 1차 치료제로 등재된 영향으로 분석된다.
[차트] HLB 주가(일봉, 최근 6개월)
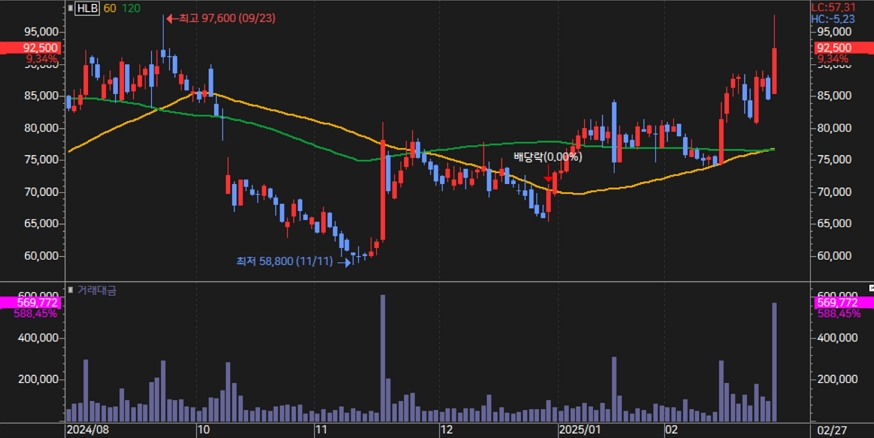
(자료: 키움증권)
ESMO의 간세포암(HCC) 진단 및 치료 가이드라인에 따르면, 리보캄렐 병용요법은 강력한 임상 근거(Level of Evidence I)를 바탕으로 간기능이 비교적 양호한 간암 환자를 위한 1차 치료제로 ‘강력 권고’됐다. 이번 개정은 2022년 이후 3년 만에 이루어진 것으로, 리보캄렐 병용요법이 기존 치료제들과 함께 대표적 치료 옵션으로 부각된 것으로 보인다.
리보캄렐 병용요법은 ‘리보세라닙(신생혈관억제제, VEGFR TKI)과 캄렐리주맙(면역항암제, anti PD-1)의 조합으로, 전체 생존 기간(mOS) 23.8개월이라는 역대 최장 데이터를 기록했다.
현재 간암 1차 치료제로 권고된 약물에는 ‘베바시주맙+아테졸리주맙’, ‘더발루맙+트레멜리무맙’ 병용요법이 포함된다. 그러나 베바시주맙 병용요법은 위장관 출혈 위험이 있어 처방 전 내시경 검사가 필요하다. 반면, 리보캄렐 병용요법은 이러한 부작용이 없어 향후 시장 점유율 확대가 기대된다.
HLB는 이번 등재가 유럽의약품청(EMA) 및 미국 FDA의 신약 승인에 긍정적인 영향을 미칠 것으로 보고 있다. 한용해 HLB 최고기술책임자(CTO)는 “국제적으로 표준 치료제 반열에 올랐다는 점에서 의미가 크다”며 “신약 허가 절차에도 긍정적인 신호가 될 것”이라고 말했다.
이번 가이드라인 개정은 미국 식품의약국(FDA)의 신약허가 결정일이 한 달도 채 남지 않은 시점에서 이루어져 더욱 주목받고 있다. ESMO 간암 관련 분과에서 발행하는 해당 가이드라인은 암 진단, 치료 및 이후 추적관리에 대한 폭넓은 정보를 제공한다. 또, 미국암종합네트워크(NCCN) 가이드라인과 함께 전 세계 전문의들이 환자 치료에 적용하는 대표적인 지침서다.
아직 신약 허가가 되지 않은 약물이 현장 의사들에게 처방을 권하는 약으로 등재된 것은 상당히 이례적이라는 평가다. 2022년 이후 3년 만에 개정된 이번 저널은 리보캄렐 병용요법이 현저한 치료 효과를 입증한 최초의 신생혈관억제(VEGFR) TKI 치료제와 면역항암제(anti PD-1)의 조합이라고 소개했다. 또, 환자 전체 생존기간(mOS)이 23.8개월에 이르는 주요 임상 데이터를 게재했다.
한편, HLB는 26일 공시를 통해 2024년 매출액이 695억원으로 전년 대비 62.2% 증가했다고 밝혔다. 영업손실은 1188억원으로 전년 대비 소폭 개선됐다. 회사 측은 이번 실적에 대해 “종속회사 및 헬스케어사업부 무형자산 손상차손 감소로 인한 이익 증가가 있었다”고 설명했다.
