이엔셀 주가는 28일 전일 대비 4.57% 상승한 1만9430원에 장을 마쳤다. 이날 주가 상승 배경에는 미국 식품의약국(FDA)으로부터 신약 파이프라인 ‘EN001’이 희귀의약품(Orphan Drug Designation, ODD)으로 지정되면서다.
[차트] 이엔셀 주가(일봉, 최근 6개월)
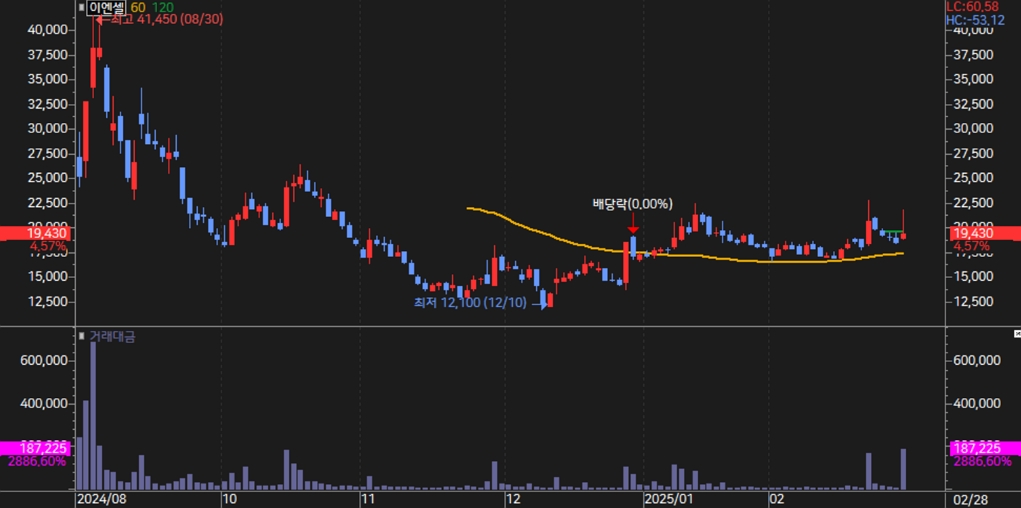
(자료: 키움증권)
EN001은 중간엽 줄기세포치료제로, 세포 노화를 억제하고 치료에 필요한 물질을 다량 분비하는 특징을 지닌다. 손상된 신경으로 이동해 치료 물질을 방출하고 신경 수초를 재생하는 역할을 한다. 현재 삼성서울병원에서 샤르코마리투스병(Charcot-Marie-Tooth, CMT) 1A형 환자를 대상으로 임상 1b상이 진행 중이다. 연구팀은 EN001을 반복 투여한 후 안전성과 유효성을 평가하고 있으며, 초기 임상 결과 중대한 이상 사례 없이 진행되고 있다.
FDA의 희귀의약품 지정으로 이엔셀은 신약 개발 과정에서 신약 허가 심사 비용 면제, 연구개발(R&D) 세금 감면, 임상 개발 지원, 시판 허가 후 7년간 시장 독점권 확보 등의 혜택을 받을 수 있게 됐다. 이로 인해 EN001이 희귀 신경질환 치료의 새로운 옵션으로 떠오르고 있다.
샤르코마리투스병은 손발 변형과 근육 위축을 유발하는 유전성 질환이다. 이 병은 현재까지 승인된 치료제가 없다. 병이 진행되면 시각과 청력 상실까지 초래할 수 있어 효과적인 치료제 개발이 시급한 상황이다.
이엔셀은 EN001을 포함해 다양한 희귀질환 치료제 개발을 적극 추진 중이다. 특히, 뒤센근위축증(Duchenne Muscular Dystrophy, DMD) 치료제도 개발 중이며, EN001을 활용한 적응증 확대 연구를 지속적으로 진행하고 있다.
이엔셀 관계자는 “EN001이 FDA의 희귀의약품 지정을 받으며 임상 진행에 더욱 탄력을 받게 됐다”며 “현재 진행 중인 임상 1b상을 순조롭게 마무리해 국내외 희귀질환 환자들에게 적기에 치료제를 공급할 수 있도록 최선을 다하겠다”고 밝혔다.